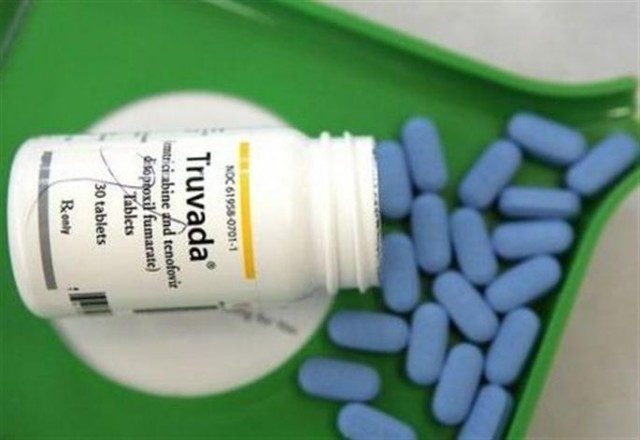
El primer tratamiento preventivo contra el SIDA para las personas con situación de riesgo, Truvada, fue aprobado en los Estados Unidos. Según las expectativas debe contribuir a reducir las nuevas infecciones. La Food and Drug Administration (FDA) de los EE.UU. aprobó esta semana la comercialización de Truvada antirretroviral que “reduciría el riesgo de transmisión del virus del sida (VIH) en sujetos sanos con alto riesgo de ser contaminados” al ser tomado diariamente.
Un panel de expertos recomendó el jueves a la (FDA) comercializar el Truvada, el primer tratamiento preventivo contra el SIDA, a pesar de los temores de algunas asociaciones sobre comportamientos sexuales más riesgosos.
Por una amplia mayoría, los 22 expertos se mostraron a favor de la comercialización del producto Truvada del laboratorio estadounidense Gilead Sciences.
Truvada, una combinación de dos medicamentos antirretrovirales, ya está prescrito para las personas infectadas con el VIH, el virus de la inmunodeficiencia humana que causa el SIDA. Su costo varía de 12,000 a 14,000 dólares al año.
La eficacia preventiva de Truvada se ha destacado por los resultados de un ensayo clínico a gran escala llevados a cabo entre julio de 2007 y diciembre de 2009 en seis países, entre ellos Brasil, Sudáfrica y los EE.UU., y financiados en gran parte por el National Institutes of Health (NIH).
El estudio demostró que se redujo en un 44% el riesgo de infección entre los hombres homosexuales que también estaban usando condones. Otro estudio clínico demostró que Truvada redujo el riesgo de infección hasta un 75% entre las parejas heterosexuales en las que uno de los dos era VIH positivo.

ese medicamento ya es muy viejo… que tiene de relevante ponerlo aqui?
una arma de dos filos!!!
@ yanimeacuerdo, totalmente de acuerdo.
con esto muchos le van a poner con ganas jajaja